DEAE-dextran
DEAE-dextran là một polycation. Ðây là tác nhân hóa học đầu tiên được sử dụng để chuyển DNA vào tế bào động vật nuôi cấy.
Trong phương pháp này, DNA ngoại lai được cho vào một trường nuôi cấy với sự có mặt của DEAE-dextran. DEAE-dextran sẽ kết hợp với DNA tích điện âm (Hình 1). Sự dư thừa điện tích dương trong phức hợp DNA-polycation do sự đóng góp của polycation, cho phép phức hợp này đi đến kết hợp chặt chẽ hơn với màng tế bào tích điện âm. Sự xâm nhập của phức hợp có thể đạt được nhờ sự nhập bào (endocytosis).
 |
| Sự kết hợp giữa DEAE-dextran và DNA |
Phương pháp kết hợp giữa DEAE-dextran và DNA
Phương pháp này được sử dụng thành công trong việc chuyển DNA vào các tế bào biểu hiện nhất thời, có nghĩa là thời gian biểu hiện ngắn chỉ vài ngày trong quá trình nghiên cứu. Tuy nhiên, phương pháp này nói chung là không hữu ích đối với các nghiên cứu cần sự chuyển nhiễm ổn định dựa vào sự hợp nhất của DNA ngoại lai vào nhiễm sắc thể, hiệu quả biến nạp thấp, chỉ được sử dụng cho một số loại tế bào và cho kết quả tốt đối với tế bào ex vivo.
Các polycation khác cũng đã được sử dụng để chuyển DNA vào tế bào như polybrene, polyethyleneimine và dendrimers.
Kỹ thuật calcium phosphate
Kỹ thuật calcium phosphate (calcium phosphate technique) đã được phát triển đầu tiên là để xác định sự lây nhiễm của DNA virus (Graham,1973) và hiện nay được sử dụng rông rãi để thử nghiệm hoạt động biến nạp của DNA virus cũng như DNA tách chiết từ các tế bào eukaryote (Wigler, 1978; Graham, 1979; Pellicer, 1980).
Kỹ thuật này yêu cầu ủ các tế bào nhận với các chất đồng kết tủa DNA và calcium phosphat (Hình 2). Kết tủa này bám vào tế bào và sau đó sẽ hấp thụ vào tế bào qua quá trình ẩm bào (Loyter, 1982). Trong tế bào, các phân tử DNA ngoại lai nằm trong không bào được tạo thành do ẩm bào và lysosome thứ hai nhưng rất ít DNA đi đến nhân vả hợp nhất vào genome chủ.
Phức hợp DNA-calcium phosphat
Cho đến nay, đây là kỹ thuật vô cùng có giá trị đối với các nghiên cứu chuyển gen vào các tế bào soma nuôi cấy và đang được sử dụng nhiều để chuyển các dòng genome vào tế bào đích. Tỉ lệ các tế bào được biến nạp ổn định của kỹ thuật này là tương đương với phương pháp vi tiêm nhưng khác với vi tiêm là nhiều tế bào được biến nạp cùng một lần. Hơn nữa, biến nạp DNA tách chiết từ các tế bào ung thư vào các tế bào nhận không ung thư đã cho thấy đây là phương pháp duy nhất để nghiên cứu sự kiểm soát di truyền của ung thư. Phương pháp này được sử dụng phổ biến bởi vì đơn giản, protocol dễ thực hiện, ít tốn kém, số tế bào chết sau biến nạp không đáng kể, sự biểu hiện gen có thể là nhất thời hoặc ổn định và quan trọng trong việc thiết kế vector virus tái tổ hợp. Tuy nhiên hiệu quả biến nạp và mức độ biểu hiện của gen chuyển thấp.
 |
| Phức hợp DNA-calcium phosphat |
Chuyển gen qua liposome
Vào thập niên 1980, liposome nhân tạo đã được sử dụng để đưa DNA vào tế bào. Lipid với toàn bộ lưới tích điện dương ở pH sinh lý là thành phần lipid tổng hợp phổ biến nhất của liposome được phát triển cho chuyển gen (Hình 3). Thường thì lipid cation được trộn với một lipid trung tính như L-dioleoyl phosphatidyl-ethanolamine (DOPE) (Hình 4). Phần cation của phân tử lipid kết hợp với DNA tích điện âm và kết quả là chứa đầy DNA trong phức hợp liposome-DNA (Hình 5). Ðối với các tế bào nuôi cấy, toàn bộ lưới tích điện dương của phức hợp liposome-DNA nói chung là gây ra hiệu quả chuyển gen cao hơn bởi vì nó cho phép phức hợp này kết hợp với màng tế bào tích điện âm bền hơn. Nhờ cơ chế nhập bào, các phức hợp xuất hiện trong endosome và sau đó đi vào nhân (Hình 2.6). Chưa rõ DNA được phóng thích từ endosome và đi qua màng nhân như thế nào. DOPE được xem là một lipid kích thích sự dung hợp và vai trò của nó là phóng thích các phức hợp này từ endosome cũng như làm cho sự dung hợp của màng tế bào phía ngoài với phức hợp liposome-DNA xảy ra dễ dàng. Trong phương pháp này, các đại phân tử trước hết được đưa vào trong các túi phospholipid. Các loại túi khác nhau đã được mô tả, nhưng túi một lớp mỏng là thích hợp nhất cho chuyển gen vì chúng có tỉ lệ khoảng trống chứa nước ở bên trong tương đối cao đối với mỗi đơn vị lipid và bởi vì chúng có tỉ lệ phân phối cao hơn. Sự dung hợp của liposome với màng plasma là một sự kiện hiếm. Hiệu quả biến nạp của phương pháp này thấp hơn so với phương pháp vi tiêm vào tiền nhân. Các nổ lực nghiên cứu đang được tiến hành để tìm ra các điều kiện thí nghiệm mà có thể làm tăng sự phóng thích các phân tử đã kết nang từ con đường ẩm bào.
 |
| Cấu trúc của DOPE (L-diolecyl phosphatidylethanolamine) |
 |
| Phức hợp liposome-DNA |
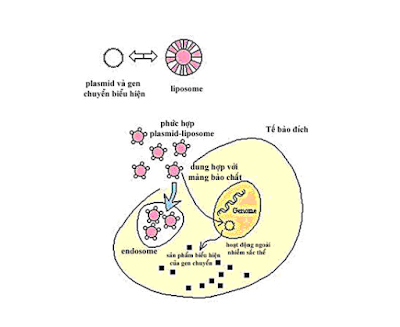 |
| Sơ đồ hoạt động của vector liposome |
Liposome đã được sử dụng để đưa protein, lipid và các phân tử nhỏ vào nhiều loại tế bào nuôi cấy, tuy nhiên hiệu quả thấp hơn vi tiêm đối với RNA hoặc protein. Cũng như thế, chuyển gen qua liposome và sự biểu hiện của gen chuyển là không vượt qua được các phương pháp chuyển gen thông thường (như hệ thống virus), sự biểu hiện gen chuyển thường nhất thời, sự ức chế bởi các thành phần của huyết thanh có thể xảy ra. Bên cạnh đó, kỹ thuật này có nhiều ưu điểm là gen chuyển sẽ không hợp nhất vào genome chủ, có hiệu quả tốt đối với cả tế bào in vitro và in vivo, có thể mang được các DNA có kích thước rất lớn, độ tinh khiết cao, không gây miễn dịch, có thể sử dụng với các tế bào mà biến nạp bằng kỹ thuật calcium phosphat không có hiệu quả..
Ứng dụng trong tương lai của kỹ thuật này chủ yếu sẽ là khả năng phân phối thuốc vào các tế bào của cơ thể sống. Hiện nay kỹ thật này đang được phát triển để cải tiến sự phân phối đặc hiệu của liposome bằng cách ghép các kháng thể đặc hiệu với bề mặt của liposome đích.
Phương pháp vi tiêm
Sự thành công đầu tiên trong nghiên cứu tạo chuột chuyển gen bằng phương pháp vi tiêm vào tiền nhân đã được công bố vào năm 1980 (Gordon, 1980). Mặc dầu cấu trúc tổ hợp gen chuyển được chứng minh là đã tích hợp vào genome của chuột, nó đã được sắp xếp lại nhưng gen ngoại lai không được biểu hiện. Các công bố tiếp theo (Brister, 1981; Costantini và Lacy; 1981) chứng minh rằng với phương pháp vi tiêm, các gen chuyển đã tích hợp và có khả năng biểu hiện. Vào năm 1982, lần đầu tiên sự thay đổi kiểu hình có thể nhìn thấy ở chuột nhắt chuyển gen đã được mô tả (Palmiter, 1982). Ðây là kết quả biểu hiện của gen hormon sinh trưởng chuột cống ở chuột nhắt. Từ đó đến nay đã có rất nhiều các công trình về chuyển gen, trong đó phần lớn là các nghiên cứu hiệu quả của gen vi tiêm với sự sinh trưởng của động vật có vú và bệnh học.
Nguyên tắc của phương pháp vi tiêm là một lượng nhỏ DNA được tiêm trực tiếp vào nhân tế bào phôi trần hoặc tế bào nguyên vẹn một cách cơ học dưới kính hiển vi. Phương pháp này cho phép đưa gen vào đúng vị trí mong muốn ở từng tế bào với hiệu quả tương đối cao.Tuy nhiên do đòi hỏi phải tinh vi, tỉ mỉ và cực kỳ chính xác nên hạn chế số lượng tế bào vi tiêm và ngoài ra còn có thể làm tổn thương đến tế bào phôi do tác nhân cơ học gây ra khi tiến hành vi tiêm.
Ðể biến nạp gen vào tế bào bằng phương pháp vi tiêm trước hết phải chế tạo kim tiêm và kim giữ. Kim được tạo ra từ những ống thuỷ tinh dẻo capillar đường kính 0,1-1,5 mm có sợi bằng wolfram mảnh ở trong nhờ hệ thống thiết bị làm kim. Hệ thống này gồm có máy kéo kim tự động (pipette puller), máy mài kim và máy gia cố kim.
 |
| Vi tiêm gen ngoại lai vào tiền nhân của trứng thụ tinh |
Ðể tạo kim tiêm trước hết phải tạo ra đầu kim nhọn nhờ máy kéo kim. Sau đó sử dụng máy gia cố để cắt đầu nhọn của ống capillar sau khi kéo tạo ra mũi kim tiêm có đường kính thích hợp. Ðường kính bên trong mũi kim tiêm tuỳ thuộc vào loại tế bào chuyển gen. Ðối với trứng tiền nhân động vật có vú có đường kính khoảng 70 µm thì đường kính của kim tiêm khoảng 0,75 µm là thích hợp, đối với phôi cá một tế bào đường kính của kim tiêm là khoảng 3-4 µm. Cuối cùng đưa kim lên máy mài để làm sắc nhọn và trơn láng đầu kim .
Kim giữ được chế tạo từ những ống capillar có đầu nhẵn bình thường để cố định trứng trong quá trình vi tiêm. Ðể tạo kim giữ, dùng máy kéo kim tự động để tạo ra đầu kim nhỏ sau đó dùng bút kim cương hoặc sợi platin đốt nóng cắt bớt đầu nhọn để tạo ra đầu kim với đường kính thích hợp. Làm nhẵn đầu kim giữ bằng cách để đứng kim này ngay trên mặt đoạn cong platin của máy gia cố. Ðốt nóng sợi platin và điều chỉnh đầu kim giữ cho nó chảy từ từ. Quan sát dưới kính hiển vi và dừng lại khi đầu kim đã đạt yêu cầu.
Vi tiêm được tiến hành trên hệ thống thiết bị vi tiêm . Hệ thống này gồm có hai bộ phận chính là kính hiển vi và máy vi thao tác.
 |
| Các máy làm kim (Hãng Narishige) |
- Máy gia cố kim Microforge
- Máy mài kim
- Máy kéo kim tự động Pipette Puller
Kính hiển vi dùng cho mục đích này là kính hiển vi soi ngược (vật kính xoay ngược lên). Ðộ phóng đại thích hợp cho việc tiến hành vi tiêm vào phôi cá một tế bào là khoảng từ 40-60 lần. Máy vi thao tác gồm 2 phần giống hệt nhau được bố trí hai bên kính hiển vi, một dùng để điều chỉnh kim tiêm, một dùng cho kim giữ. Tính năng của máy này là cho phép điều chỉnh các kim theo không gian 3 chiều. Kim tiêm và kim giữ được lắp vào máy vi thao tác và được nối với syringe qua ống bằng chất dẻo được nạp đầy dầu parafin.
Chuẩn bị dung dịch gen chuyển: gen chuyển được xen vào trong một vector plasmid và tạo dòng trong E.coli. Các vi khuẩn biến nạp mang plasmid tái tổ hợp được phát hiện trong môi trường nuôi cấy có thuốc kháng sinh do plasmid mang các gen kháng thuốc đặc hiệu. Các vi khuẩn sống sót được sinh trưởng trong môi trường dinh dưỡng thích hợp và plasmid tái tổ hợp mang gen chuyển sẽ được sao chép mỗi khi tế bào vi khuẩn phân chia. Sau đó, hàng triệu bản sao của plasmid tái tổ hợp mang gen chuyển được tách chiết từ các tế bào vi khuẩn này và các đoạn gen chuyển được tách ra từ plasmid tái tổ hợp nhờ sử dụng enzym hạn chế. Ðể tinh sạch, gen chuyển được điện di trên gel agarose. Hoà tan gen chuyển trong dung dịch đệm đặc trưng (như dung dịch Tris-EDTA; dung dịch TE...) và tính nồng độ dung dịch gen chuyển nhờ quang phổ kế. Nồng độ dung dịch DNA sử dụng cho vi tiêm thường là 1-5 µg/ml. Trước khi chuyển vào phôi, gen chuyển được kiểm tra sự biểu hiện trong các tế bào nuôi cấy bằng sự chuyển nhiễm (transfection).
 |
1. Kính hiển vi soi ngược 2. Máy vi điều chỉnh
Vi tiêm được tiến hành qua các bước: nạp gen vào kim tiêm bằng phương pháp capillar (ngâm đầu kim tiêm vào dung dịch gen khoảng 10-12 giờ) hoặc bơm trực tiếp dung dịch gen vào, lắp kim tiêm và kim giữ vào máy vi thao tác, chuyển trứng tiền nhân vào đĩa petri có chứa môi trường được đặt dưới kính hiển vi, giữ trứng tiền nhân vào đầu kim giữ bằng lực hút của syringe, điều chỉnh kính hiển vi để xác định đĩa phôi và điều chỉnh máy vi thao tác để đưa kim tiêm vào vị trí của trứng tiền nhân, đẩy gen vào trứng tiền nhân bằng cách vặn nhẹ syringe. Khi thấy trứng tiền nhân hơi phồng to và trở nên sáng hơn thì dừng lại và kéo nhanh kim tiêm ra. Trứng tiền nhân sau khi tiêm được di chuyển xa đến cuối đĩa petri trước khi tiêm trứng tiền nhân tiếp theo. Mỗi một nhóm trứng tiền nhân đã hoàn thành được chuyển sang một đĩa môi trường khác để ấp và đánh giá bằng mắt trong một vài tiếng. Sau đó tất cả các trứng tiền nhân được nhìn thấy rõ ràng và được chuyển vào ống dẫn trứng của con cái nhận.
Cho đến nay, trong các kỹ thuật chuyển gen vào động vật thì phương pháp vi tiêm dung dịch DNA vào hợp tử là phương pháp có hiệu quả nhất trên động vật có vú và hiện là phương pháp chủ yếu được sử dụng để chuyển gen vào vật nuôi.
Ðối với thực vật thì phương pháp này được sử dụng đối với các tế bào tiền phôi của hợp tử hoặc các tế bào tiền phôi của hạt phấn.
Tuy nhiên sự xâm nhập của gen chuyển vào DNA tế bào vật chủ là một quá trình ngẫu nhiên và xác suất để gen chuyển xen vào vị trí DNA vật chủ mà sẽ cho phép nó biểu hiện là thấp. Hiệu quả của vi tiêm là không cao (Bảng 1).
(Hammer và cộng sự, 1985)
Hiệu quả vi tiêm ở một số loài động vật
|
Loài động vật
|
Số lượng
trứng được vi tiêm
|
Số lượng
con sinh ra từ trứng vi tiêm
|
Số lượng
con chuyển gen
|
|
Thỏ
|
1907
|
218 (11,4%)
|
28 (1,5%)
|
|
Cừu
|
1032
|
73 (7,1%)
|
1(0,1%)
|
|
Lợn
|
2035
|
192 (9,4%)
|
20 (1%)
|
 |
| Chuyển gen bằng vi tiêm |
Phương pháp chuyển gen nhờ vector virus
Vào năm 1974, lần đầu tiên các nhà khoa học phát hiện thấy rằng, sau khi tiêm DNA của retrovirus SV40 vào khoang phôi (blastocoel) của túi phôi chuột, DNA này có thể được tìm thấy sau đó trong các tế bào của chuột trưởng thành (Jaenisch,1974; Jaenisch và Mintz,1974). DNA provirus Mo-Mulv sử dụng trong các thí nghiệm như thế này đã tích hợp vào genome và truyền lại cho thế hệ sau, do đó đã tạo nên các dòng chuột ổn định (Stuhlmann, Jahner và Jaenisch,1981). Từ đó, việc sử dụng virus làm vector cho các DNA ngoại lai đã được phát triển.
Phương pháp này tuy thao tác hơi phức tạp nhưng có ưu điểm là hiệu quả chuyển gen cao. Hơn nữa gen cấu trúc gắn vào vector virus sẽ sử dụng promoter của virus, các promoter này thường có hoạt tính cao do đó gen cấu trúc này sẽ được biểu hiện mạnh trong tế bào chủ.
Về nguyên tắc, bất kỳ loại virus nào cũng có thể được sử dụng làm vector để chuyển vật liệu di truyền vào trong tế bào. Nhiều nhóm trong số đó, các papovavirus, adenovirus, retrovirus...được sử dụng vào những mục đích chuyên biệt. Ðể sử dụng làm vector, các phần khác nhau của genome virus được thay thế bằng gen cấu trúc quan tâm. Virus có thể được sử dụng để lây nhiễm vào tế bào giai đoạn sớm của phôi trước khi được chuyển ghép vào con mẹ. Gen chuyển với vector retrovirus xâm nhập một cách hiệu quả vào hệ gen của vật chủ nhưng virus sử dụng phải là virus an toàn, không gây bệnh.
Các cơ thể chuyển gen sinh ra từ phương pháp này là ở dạng khảm, có nghĩa là không phải tất cả các tế bào của cơ thể đều mang retrovirus. Gen chuyển chỉ có thể di truyền được nếu retrovirus hợp nhất vào một số tế bào sinh dục. Ðối với phương pháp này tỉ lệ sống của các động vật chuyển gen sơ sinh là rất thấp. Nếu như các thao tác di truyền là chuẩn xác, không gây ra sự sẩy thai, thì thế hệ động vật đầu tiên (F1) cần kiểm tra sự biểu hiện của gen chuyển. Khi gen chuyển đã hợp nhất trong các tế bào sinh dục thì được gọi là thể khảm dòng mầm và sau đó chúng được lai cùng dòng khoảng 10-20 thế hệ cho đến khi thu được các động vật chuyển gen đồng hợp tử và gen chuyển có mặt ở trong tất cả mọi tế bào. Ở giai đoạn này, phôi mang gen chuyển có thể được đông lạnh và được bảo quản cho các quá trình cấy chuyển về sau.
 |
| Chuyển gen nhờ vector là virus |
Chuyển gen bằng cách sử dụng tế bào gốc phôi
Xuất phát từ lý do các tế bào gốc phôi (tế bào phôi ở giai đoạn 16-32 tế bào) là các tế bào đa năng (totipotent) nghĩa là có thể phân hoá thành bất kỳ loại mô nào và từ đó sẽ tạo nên cơ thể hoàn chỉnh. Từ các túi phôi nuôi cấy in vitro, người ta đã tiến hành tách chiết các tế bào gốc phôi và biến nạp gen ngoại lai vào những tế bào này.
Sau khi chọn ra những tế bào đã được biến nạp gen lạ người ta đưa nó vào phôi khác ở giai đoạn phôi nang để tạo ra động vật chuyển gen thể khảm. Trên 30% động vật chuyển gen tạo thành là những động vật chuyển gen thể khảm dòng mầm mang kiểu gen của dòng tế bào này. Ở đây các tế bào gốc phôi được sử dụng như là một phương tiện để chuyển gen (Mintz, 1977).
Ưu điểm của phương pháp chuyển gen này là tỉ lệ phôi sống sót sau thao tác, sự tích hợp và biểu hiện tính trạng của gen mới khá cao. Ðiều quan trọng hơn là trong thực tế việc chuyển gen có thể được tiến hành thông qua sự thao tác với phôi dâu và túi phôi. Phôi ở các giai đoạn này có thể thu nhận mà không cần phẫu thuật (đặc biệt là đối với bò), do vậy công việc chuyển gen được tiến hành rất dễ dàng.
Phương pháp này có ý nghĩa đặc biệt đối với sự nghiên cứu kiểm tra di truyền của các quá trình phát triển. Sự thuận lợi của nó là cho phép tạo ra một cách chính xác các đột biến gen xác định bằng tái tổ hợp đồng dạng.
Trong tương lai phương pháp sử dụng tế bào gốc phôi sẽ được sử dụng rộng rãi để tạo động vật chuyển gen.
Có ba cách tạo động vật chuyển gen từ các tế bào gốc phôi mang gen chuyển:
-Thứ nhất, phương pháp được dùng trước mắt là bơm một số tế bào gốc phôi (khoảng 5-10 tế bào) vào trong xoang phôi nang của tế bào động vật.
-Thứ hai, xen một số tế bào gốc phôi vào giữa bào thai thời kỳ 8 tế bào.
-Thứ ba, nuôi cấy chung tế bào gốc phôi với phôi qua đêm.
 |
| Phương pháp chuyển gen bằng cách sử dụng tế bào gốc phôi |
 |
| Chuyển tế bào gốc phôi vào túi phôi |
Chuyển gen trực tiếp vào protoplast
Ðể DNA dễ xâm nhập được vào tế bào thực vật, phải loại bỏ vách tế bào tạo protoplast. Protoplast có thể được duy trì trong môi trường nuôi cấy như các tế bào sinh trưởng một cách độc lập hoặc với một môi trường đặc hiệu, vách tế bào có thể được tạo thành và toàn bộ các cây có thể được tái sinh từ các tế bào này. Quá trình chuyển gen như thế này được thực hiện một cách trực tiếp bằng một cơ chế vật lý đơn giản, không cần có vector.
Ðể nâng cao hiệu quả biến nạp, người ta đã đã xử lý protoplast với PGE (polyethylene glycol) hoặc bằng xung điện.
Phương pháp chuyển gen này rất có hiệu quả, đặc biệt đối với những loài thực vật mà phương pháp chuyển gen gián tiếp nhờ Agrobacterium không thể thực hiện được. Tuy nhiên, việc tạo protoplast cũng như tái sinh cây từ protoplast không đơn giản, tốn nhiều công sức, bị ảnh hưởng của nhiều yếu tố môi trường. Với phương pháp này, các nhà khoa học đã chuyển gen thành công vào một số loài cây một lá mầm như loài lúa phụ Japonica (Datta, 1990), ngô (Doon, 1990), lúa mì (Vassil, 1992).
Chuyển gen bằng kỹ thuật xung điện
Kỹ thuật xung điện (electroporation) là một phương pháp cơ học được sử dụng để đưa các phân tử phân cực vào trong tế bào chủ qua màng tế bào. Trong phương pháp này, một xung điện cao thế trong khoảnh khắc (vài phần nghìn giây) có khả năng làm rối loạn cấu trúc màng kép phospholipid, tạo ra các lỗ thủng tạm thời cho phép các phân tử DNA ngoại lai từ môi trường xâm nhập vào bên trong tế bào.
Nhiều kỹ thuật nghiên cứu trong sinh học phân tử yêu cầu đưa gen hoặc protein ngoại lai vào trong tế bào chủ. Vì lớp phospholipid kép của màng sinh chất có một đầu ưa nước phía ngoài và một đầu ưa nước phía trong , nên bất kỳ phân tử phân cực nào, bao gồm cả DNA và protein, đều không có khả năng đi qua màng một cách tự do (Farabee, 2001).
 |
| Sơ đồ màng phospholipid kép |
Sơ đồ này cho thấy các thành phần hóa học của màng sinh chất. Các đầu ưa nước phân cực hướng về phía ngoài trong khi các đuôi kỵ nước hướng về phía trong và tương tác với đuôi kỵ nước khác để cùng bám giữ màng. Các phân tử phân cực không thể đi qua màng này nếu như không có sự hỗ trợ bên ngoài.
Nhiều phương pháp đã được phát triển để vượt qua rào cản này, cho phép đưa DNA và các phân tử khác vào trong tế bào đã được nghiên cứu. Một trong những phương pháp này là kỹ thuật xung điện.
Kỹ thuật xung điện dựa trên trạng thái tương đối yếu của các tương tác kỵ nước của phospholipid kép và khả năng tập hợp lại một cách tự động của nó sau khi bị rối loạn (Purves, 2001). Vì vậy, một xung điện chớp nhoáng có thể gây ra rối loạn ở các vị trí của màng một cách nhất thời, làm cho các phân tử phân cực có thể đi qua, nhưng sau đó màng có thế đóng kín lại nhanh chóng và tế bào không bị ảnh hưởng gì cả.
Các tế bào chủ và DNA ngoại lai được tạo thành dịch huyền phù và cho vào trong một cuvette nhựa có điện cực (Hình dưới).
 |
| Cuvette nhựa có điện cực |
Hình 2.15: Cuvette nhựa có điện cực
Ðể tạo ra xung điện cao thế trong một thời gian ngắn người ta sử dụng một thiết bị gọi là máy xung gen (gene pulser) (Hình 2.16). Quá trình cơ bản diễn ra bên trong máy này có thể được trình bày bằng sơ đồ hình 2.17.
 |
| Máy xung gen (Gene pulser) (Hãng Biorad) |
 |
| Sơ đồ bố trí mạch cơ bản của máy xung điện |
Sơ đồ này cho thấy mạch điện cơ bản cung cấp điện cho kỹ thuật xung điện
Khi công tắc thứ nhất đóng, tụ điện nạp điện vào và tích một điện áp cao. Khi công tắc thứ hai đóng, điện áp này phóng qua dịch huyền phù tế bào. Một xung điện cần thiết cho kỹ thuật này thường là khoảng 10.000-100.000 v/cm (thay đổi tùy theo kích thước của tế bào) trong vài phần triệu giây đến một phần ngàn giây. Xung điện này làm rối loạn phospholipid kép của màng tế bào và tạo ra các lỗ tạm thời. Khả năng điện qua màng tế bào cùng lúc tăng lên 0,5-1,0 v vì vậy các phân tử đã được nạp điện này đi qua màng tế bào thông qua các lỗ bằng cách thức tương tự như điện di (Hình dưới).
 |
| Sơ đồ plasmid chứa DNA ngoại lai đi qua các lỗ tạm thời trên màng bào chất |
Lối DNA đi vào tế bào không thể quan sát thấy dưới kính hiển vi, nhưng hình vẽ này cho thấy khái niệm cơ bản của sự tạo thành các lỗ trên màng mà DNA có thể đi qua.
Khi các ion đã nạp điện và các phân tử đi qua các lỗ, màng tế bào phóng điện và các lỗ này đóng lại một cách nhanh chóng và phospolipid kép phục hồi lại cấu trúc cũ (Weaver, 1995). Lúc này các phân tử mong muốn đã ở trong tế bào và chúng được sử dụng cho các nghiên cứu tiếp theo.
Phương pháp này có thể sử dụng đối với gần như tất cả các loại tế bào của các loài. Lúc đầu phương pháp này được sử dụng để chuyển gen vào các tế bào động vật có vú, về sau cho cả tế bào thực vật ở dạng protoplast... Với một số cây một lá mầm quan trọng (loài lúa phụ Japonica, ngô, lúa mì) mà không thể thể thực hiện được bằng phương pháp chuyển gen gián tiếp nhờ Agrobacterium thì người ta đã thành công với phương pháp này. Hiệu quả biến nạp cao. Trong một nghiên cứu ở E.coli, 80% số tế bào nhận được DNA ngoại lai (Miller và Nickoloff, 1995). Lượng DNA ngoại lai cần thiết là ít hơn so với các phương pháp khác (Withers, 1995). Phương pháp này có thể thực hiện với các mô in vivo còn nguyên vẹn (Weaver, 1995). Ðoạn DNA ngoại lai được biến nạp có kích thước lớn. Tuy nhiên nếu các xung điện có cường độ và chiều dài không đúng thì một số lỗ của tế bào sẽ trở nên quá lớn hoặc bị hỏng không thể đóng lại sau khi tế bào phóng điện, làm cho tế bào bị tổn thương hoặc bị thủng (Weaver, 1995). Một hạn chế nữa là sự vận chuyển DNA ngoại lai vào và ra khỏi tế bào trong suốt thời gian điện biến nạp là tương đối không đặc hiệu. Ðiều này dẫn đến kết quả là không cân bằng ion mà sau đó sẽ làm rối loạn chức năng của tế bào và tế bào chết (Weaver, 1995).
Kỹ thuật xung điện được sử dụng rộng rãi trong nhiều lĩnh vực khác nhau của sinh học phân tử và y học. Các ứng dụng của kỹ thuật xung điện bao gồm:
- Biến nạp DNA: các gen đặc hiệu có thể được tạo dòng trong plamid và sau đó plasmid này được đưa vào tế bào chủ để nghiên cứu cấu trúc và chức năng của gen và protein.
- Chuyển plasmid trực tiếp giữa các tế bào: tế bào vi khuẩn đã chứa plasmid có thể được ủ với một dòng khác không mang plasmid nhưng lại có đặc tính mong muốn khác. Ðiện áp của xung điện sẽ tạo ra các lỗ, cho phép một số plasmid đi ra khỏi tế bào và lại đi vào tế bào khác. Sau đó các tế bào mong muốn sẽ được chọn lọc bằng tính kháng thuốc kháng sinh hoặc bằng phương pháp tương tự khác (Withers, 1995). Kiểu chuyển gen này cũng có thể được thực hiện giữa các loài khác nhau. Vì vậy, một lượng lớn plasmid sinh trưởng trong các khuẩn lạc vi khuẩn được nhân lên một cách nhanh chóng và sau đó được chuyển vào các tế bào nấm men bằng kỹ thuật xung điện để nghiên cứu (Gunn, 1995).
- Dung hợp tế bào đã kích thích: sự tạo thành các lỗ thủng trên màng xảy ra do xung điện chớp nhoáng tạo ra cho thấy đã kích thích sự dung hợp tế bào (Weber và Berrg, 1995).
- Phân phối thuốc qua da: Chỉ khi xung điện gây ra các lỗ tạm thời trên màng sinh chất, các lỗ tương tự đã tạo ra ở màng lipid kép của lớp da chết ở phía ngoài cùng. Các lỗ này cho phép thuốc đi qua da đến các mô đích. Các bệnh nhân thích phương pháp này hơn phương pháp tiêm (không cần kim tiêm) và có thể tránh được các vấn đề phân hủy hoặc hấp thu không đúng của liệu pháp uống thuốc (oral medication) trong hệ tiêu hóa (Praustmitz, 1993).
- Liệu pháp hóa điện khối u ung thư (cancer tumor electrochemotherapy): các nhà khoa học đang nghiên cứu tiềm năng của kỹ thuật xung điện để tăng tính hiệu quả của liệu pháp hóa học. Khi sử dụng kỹ thuật xung điện để biến nạp DNA, xung điện này sẽ phá vỡ màng tế bào ung thư và làm tăng lượng thuốc đi đến các vị trí. Một số nghiên cứu cho rằng đã làm giảm sự phát triển khối u khi áp dụng phương pháp này cho các tế bào ung thư ở hệ thống mô hình động vật (Maeda, 1998).
- Liệu pháp gen: kỹ thuật xung điện cho phép các vector mang các gen quan tâm được biến nạp qua da đến các mô đích. Khi đã hợp nhất vào các tế bào của cơ thể, các protein được tổng hợp từ các gen này có thể thay thế gen sai hỏng và vì vậy đã điều trị các rối loạn di truyền (Hình dưới)(Inovio, 2002).
 |
| Ứng dụng của kỹ thuật xung điện trong liệu pháp gen |
Chuyển gen bằng súng bắn gen
Súng bắn gen (Gene gun) là một thiết bị sử dụng để đưa thông tin di truyền vào tế bào, được thiết kế đầu tiên cho biến nạp DNA ngoại lai vào tế bào thực vật và được phát triển vào đầu thập niên 1980 do các nhà thực vật học ở Ðại học Corrnell cùng với các nhà nghiên cứu ở Corrnell Nanofabrication Facility, Newyork, USA. Súng bắn gen được bán trên thị trường vào năm 1990. Ðạn sử dụng cho loại súng này là các hạt kim loại nặng cơ bản được bao bọc DNA. Tên chính xác và đầy đủ của súng bắn gen là hệ thống phân phối hạt biolistics (biolistic particle delivery system) và kỹ thuật này thường được gọi một cách đơn giản là biolistics (sự kết hợp giữa hai thuật ngữ biology (sinh học) và ballistics (sự bắn tung)). Mặc dù có nhiều thiết kế kỹ thuật khác nhau nhưng nguyên lý chung của phương pháp này là sử dụng áp lực xung của khí helium để gai tốc các hạt.
 |
| Ứng dụng của kỹ thuật xung điện trong liệu pháp gen |
Súng bắn gen bao gồm hai buồng bằng thép không gỉ, kích thước 6“x7“x10“ nối với hai bơm chân không. DNA ngoại lai được gắn vào các hạt tungsten có đường kính rất nhỏ, khoảng 1μm (các kim loại năng khác như vàng và bạc cũng được sử dụng nhưng không thường xuyên do giá cả đắt). Các hạt này được đặt trên một cái đĩa ở mặt bên trong của súng. Sự bùng nổ khí helium ở 1000psi làm cho cái đĩa bắn về phía trước với tốc độ 1300 food/s, tương đương với tốc độ khi một viên đạn rời khỏi nòng súng. Một tấm chắn làm dừng đĩa lại và các hạt vàng hay tungsten được phóng về phía các tế bào đích. Chúng xuyên qua vách tế bào và phóng thích các phân tử DNA (Hình 2.21). Súng bắn gen sử dụng kỹ thuật DNA tái tổ hợp để hợp nhất sự biểu hiện các gen đã phân phối. Các tế bào biến đổi di truyền có thể được sử dụng để tạo thực vật bao gồm cả sự sửa đổi di truyền mong muốn ở trong tất cả các tế bào của chúng (Voiland, 1999).
 |
| Sơ đồ nguyên lý hoạt động của súng bắn gen |
Mục tiêu của súng bắn gen thường là callus của các tế bào thực vật giống nhau sinh trưởng trong môi trường gel trên đĩa petri. Sau khi các hạt tungsten đã va chạm vào đĩa, gel và callus bị phá vỡ nhiều. Tuy nhiên một số tế bào không bị phá vỡ khi va chạm mạnh và đã tiếp nhận các hạt tungsten được bao bọc DNA và cuối cùng các phân tử DNA ngoại lai đã xâm nhập và hợp nhất vào nhiễm sắc thể thực vật. Các tế bào từ đĩa petri được tập hợp lại và chọn lọc các tế bào đã hợp nhất thành công và biểu hiện DNA ngoại lai bằng các kỹ thuật hóa sinh hiện đại như sử dụng gen chọn lọc nối tiếp và Northern blots.
Các tế bào đơn đã chọn lọc từ callus có thể được xử lý với một số hormone thực vật như auxin, gibberelin và mỗi một tế bào có thể phân chia, biệt hóa thành các tế bào mô, cơ quan, tế bào chuyên hóa của toàn bộ cây. Cây mới có nguồn gốc từ một tế bào nảy mầm thành công có thể mang các đặc tính di truyền mới
 |
| Chuyển gen bằng súng bắn gen |
Phương pháp này có ưu điểm là thao tác dễ dàng, có thể chuyển gen vào nhiều loại tế bào và mô, các tế bào được biến nạp có tỉ lệ sống sót cao, cho phép đưa các gen vào tế bào ở vị trí mong muốn....Do vậy nó được sử dụng rộng rãi trong nhiều lĩnh vực. Các ứng dụng của kỹ thuật bắn gen bao gồm
- Tạo thực vật chuyển gen: đây là phương pháp được sử dụng rộng rãi nhất hiện nay trong lĩnh vực tạo ngũ cốc chuyển gen. Bacillus thuringiensis là loài vi khuẩn tổng hợp ra protein crystal (crys1Ab và crys1Ac) có khả năng giết một cách chọn lọc các nhóm côn trùng nhất định. Gen mã hoá protein crystal được gọi là gen Bt. Gen Bt đã được bắn vào mô sẹo của cây ngũ cốc (Rassmussen, 1994). Trong khi các tế bào này sửa chữa tổn thương, DNA ngoại lai xâm nhập vào genome tế bào chủ. Vì vậy cho phép tế bào chủ phiên mã và giải mã gen Bt. Sau mỗi lần quá trình biến nạp được hoàn thành người ta cũng tiến hành sàng lọc theo phương pháp truyền thống là dựa trên cơ sở các marker chọn lọc được xen vào DNA cấu trúc (Brettschneider, 1997). Các marker chọn lọc mang tính kháng (kháng thuốc kháng sinh hay kháng thuốc diệt cỏ) như kanamycin là một là một trong những marker phổ biến nhất được sử dụng.
- Tiêm chủng vaccine di truyền: các gen được đưa vào cơ thể bằng súng bắn gen với mục đích gây ra phản ứng miễn dịch với protein biểu hiện bởi gen chuyển. Phương pháp tiêm chủng vaccine này an toàn hơn các phương pháp khác bởi vì chỉ DNA ngoại lai được đưa vào và không có các protein ngoại lai (Lin, 2000).
- Liệu pháp gen tự sát (Suicide gene therapy): phương pháp bắn gen đã được sử dụng trong điều trị bệnh ung thư. Một gen biểu hiện protein gây độc có promoter đặc hiệu khối u được đưa vào các tế bào khối u. Khi protein này được biểu hiện thì tế bào khối u chết. Protein này chỉ gây độc đối với các tế bào khối u bởi vì promoter đặc hiệu cần cho sự biểu hiện chỉ được tạo ra trong các tế bào khối u (Lin, 2000).
- Sự điều biến miễn dịch (Immunomodulation): phương pháp này còn được sử dụng để chống lại ung thư. Sử dụng súng bắn gen, một protein chỉ biểu hiện trong tế bào khối u nhưng làm cho phản ứng miễn dịch tăng lên được đưa vào tế bào. Phản ứng miễn dịch tăng lên nhắm vào các tế bào khối u và hiển nhiên gây ra hiệu quả mong muốn (Lin,2000).
- Dược lý di truyền: súng bắn gen có thể được sử dụng để đưa các gen tổng hợp protein hữu ích hay protein liệu pháp vào cơ thể. Ví dụ như các yếu tố đông máu ở các cơ thể rối loạn sự đông máu hoặc tăng sự tổng hợp hồng cầu trong các cơ thể thiếu máu. Sự biểu hiện kéo dài của các gen đưa vào là một vấn đề, trong nhiều trường hợp thường đòi hỏi sự phân phối gen phức tạp (Lin, 2000).
- Súng bắn gen là một công cụ nghiên cứu: súng bắn gen có thể được sử dụng để xen các promoter mà sẽ dẫn đến sự biểu hiện của các gen nhất định. Hiệu quả khuyếch đại các protein nhất định là một phương pháp có giá trị lớn đối với các nhà khoa học để nghiên cứu chức năng của các protein này (Lin, 2000).
Phương pháp chuyển gen gián tiếp nhờ Agrobacterium
Agrobacterium có khả năng xâm nhiễm tế bào thực vật bằng cách chuyển một đoạn DNA của nó vào tế bào thực vật. Khi DNA vi khuẩn được hợp nhất với nhiễm sắc thể thực vật, nó sẽ tấn công vào hệ thống tổ chức của tế bào một cách có hiệu quả và sử dụng nó để đảm bảo cho sự sinh sôi của quần thể vi khuẩn. Thật không may mắn cho các nhà trồng cây ăn quả khi gặp phải loài vi khuẩn này. Bởi vì nó chính là thủ phạm gây ra bệnh khối u hình chóp và bệnh lông rễ ở nhiều loài cây cảnh và cây ăn quả.
Mặc dù hệ thống chuyển gen gián tiếp nhờ Agrobacterium là có hiệu quả đối với một số loài nhưng không phải tất cả thực vật có thể được biến nạp bằng con đường này. Ðặc biệt, lớp một lá mầm bao gồm các cây ngũ cốc chính trên thế giới như lúa, lúa mì và ngô là không được biến nạp dễ dàng nhờ A. tumefaciens.
Ðể khai thác và sử dụng A. tumefaciens như là một vector chuyển gen các nhà khoa học đã loại bỏ các gen gây khối u và gen mã hoá opine của T - DNA và thay thế vào đó là các marker chọn lọc, trong khi vẫn duy trì các vùng bờ phải và bờ trái của T-DNA và các gen vir. Gen chuyển được xen vào giữa các vùng bờ của T-DNA. Nó sẽ được chuyển vào tế bào và trở nên hợp nhất với nhiễm sắc thể tế bào thực vật
Phương pháp chuyển gen gián tiếp nhờ Agrobacterium đã được kiểm tra đối với sự xâm nhập bền vững, sự biểu hiện và sự di truyền của các gen chuyển đặc biệt. Tuy nhiên, một vài yếu tố ảnh hưởng đến hiệu quả biến nạp là loại mô được biến nạp, giai đoạn phát triển của mô, mức độ khởi đầu của vi khuẩn A. tumefaciens sử dụng, môi trường để nuôi cấy mô sau khi biến nạp, marker được sử dụng để chọn lọc thể biến nạp, loại vector sử dụng và kiểu gen của thực vật.
 |
| Tạo thực vật chuyển gen bằng phương pháp chuyển gen gián tiếp nhờ Agrobacterium |
Chuyển gen vào tinh trùng và các tiền thể của tinh trùng
Chuyển gen vào tinh trùng
Tinh trùng trưởng thành có genome bất hoạt không có khả năng tái bản. DNA của nó được bao phủ bởi protamine làm cho DNA ngoại lai rất khó đi vào trong genome tinh trùng. Vì vậy DNA ngoại lai không có cơ hội để hợp nhất vào DNA tinh trùng.
Các thí nghiệm thực hiện cách đây khoảng gần một thập kỷ cho thấy rằng tinh trùng ủ với DNA có thể mang DNA đến trứng trong quá trình thụ tinh dẫn đến kết quả là tạo ra chuột chuyển gen. Các nghiên cứu hóa sinh học cho thấy DNA bám vào tinh trùng một cách dễ dàng nhưng không chứng minh được rằng điều này xảy ra do sự xâm nhập của DNA. Vì thế tinh trùng đóng vai trò là một thể truyền đối với DNA ngoại lai.
Sau một vài năm, phương pháp này được áp dụng rộng rãi với bò, lợn, cừu và cá medaka (Hình 2.24). Trong tất cả các trường hợp này không hiểu tại sao các thí nghiệm rất khó thành công. Hơn nữa, phần lớn các trường hợp, DNA ngoại lai hợp nhất vào genome vật chủ đã được sắp xếp lại ở mức độ cao. Một nghiên cứu đã cho thấy rằng ngay cả sau khi đã rửa cẩn thận, tinh trùng chứa DNAse đã phân hủy DNA ngoại lai. DNAse có rất nhiều trong nguyên sinh chất của tinh trùng và lượng enzyme này bám vào tinh trùng là thay đổi đã giải thích tại sao thí nghiệm này không thành công và tại sao DNA ngoại lai bị phân cắt. DNA ngoại sinh dường như gây ra hoạt tính DNAse ở tinh trùng đã tách chiết ra. Có thể giải thích hiện tượng này là DNAse một phương tiện để bảo vệ tinh trùng tránh khỏi sự nhiễm DNA ngoại sinh trên đường từ mào tinh hoàn đến tế bào trứng (Baccetti và Spadafora, 2000).
Các thử nghiệm để tăng DNA xâm nhập vào tinh trùng đã được thực hiện. Sự xung điện hoặc chuyển nhiễm với các tác nhân hóa học đã làm tăng sự hấp thu DNA vào tinh trùng. Hiện tượng này thường được kèm theo do khả năng thụ tinh cho bào trứng của tinh trùng.
Ở Xenopus, chuyển gen vào phôi bằng vi tiêm dẫn đến sự biểu hiện của gen ngoại lai và nó tồn tại từ vài ngày đến vài tuần nhưng lại không hợp nhất vào genome vật chủ. Ðể khắc phục khó .
 |
| Chuyển gen vào tinh trùng |
Tinh trùng đã rửa ủ với DNA được sử dụng để thụ tinh in vivo hoặc in vitro. Phương pháp này không có hiệu quả đặc hiệu đối với việc tạo động vật chuyển gen và các gen đã hợp nhất thường bất hoạt do sự sắp xếp lại DNA
Màng tinh trùng bị tổn thương bởi chất tẩy nhẹ. DNA ngoại lai đi vào tinh trùng một cách tự do. Các tinh trùng này được sử dụng để thụ tinh in vitro bằng phương pháp ICSI khăn này, các nhà nghiên cứu đã sử dụng tinh trùng làm thể mang (carrier). Protocol đã được xác định sớm hơn cho động vật có vú đã chứng tỏ không hiệu quả ở Xeponus. Ðể tăng khả năng hấp thu DNA, tinh trùng được xử lý với Triton, một chất tẩy nhẹ. Ðiều này dẫn đến sự không ổn định của màng tinh trùng làm cho DNA tự do đi vào tinh trùng. Kết quả tương tự cũng đạt được khi làm lạnh và ấm tinh trùng. Chromatin đã bị phân hủy do enzyme hạn chế nhận biết một vài vị trí ở chromatin của tinh trùng nhưng đối với DNA ngoại lai thì không xảy ra. Ðiều này gây ra cơ chế sửa chữa và làm tăng cơ hội hợp nhất DNA ngoại lai vào genome của phôi. Phương pháp này có tên gọi là REMI (restriction enzyme mediated intergration=sự hợp nhất qua trung gian ezyme hạn chế), một phương pháp làm tăng sự biến nạp của tế bào. Sau các xử lý này, tinh trùng mất khả năng thụ tinh cho trứng. Tiêm trực tiếp tinh trùng vào trứng (intra-cytoplasmic sperm ịnjection=ICSI) được sử dụng đối với sự thụ tinh in vitro ở người. Phương pháp này đã được áp dụng cho Xeponus và đã tạo ra Xeponus chuyển gen với kết quả có thể chấp nhận (Hình 2.12B). Ðặc biệt hiện nay các nhà sinh học đã ứng dụng chuyển gen vào loài này để nghiên cứu sự phát triển (Marrsh-Arrmstrong, 1999; Perrny, 2001).
Phương pháp này, trước tiên được sử dụng cho Xeponus, đã chứng tỏ thành công ở chuột. Tuy nhiên nó không cho kết quả cao hơn phương pháp vi tiêm vào tiền nhân là một phương pháp đơn giản hơn nhiều. Phương pháp ISCI đã được sử dụng thành công hoàn toàn ở chuột khi chuyển các đoạn DNA dài được thiết kế trong các vector BAC và YAC (Perry, 2001). Vì vậy phương pháp này có thể được áp dụng rộng rãi đối với các loài khác kể cả gia súc lớn. Hiện nay hạn chế của việc sử dụng ICSI ở các loài này là khó khăn. Dường như là không thể áp dụng với các loài không thuộc bộ Linh trưởng mà việc chuyển gen là khó khi sử dụng các phương pháp khác.
Gần đây, một phương pháp tuyệt vời đã được đề xuất (Qian, 2001). DNA bám vào kháng thể đơn dòng nhận biết một protein trên bề mặt tinh trùng hình thành nên một phức hợp ổn định với tinh trùng. Phương pháp này đã được sử dụng để thụ tinh in vitro ở chuột, gà bằng thụ tinh nhân tạo và lợn bằng cách tiêm vào sừng tử cung. Trong ba trường hợp này, khoảng 30% cá thể con sinh ra là động vật chuyển gen. Gen chuyển đã không bị sắp xếp lại. Nó đã biểu hiện và truyền lại cho thế hệ sau. Ðiều quan tâm là kháng thể đơn dòng giống nhau nhận biết tinh trùng của động vật có xương sống thấp hơn và cao hơn kể cả con người. Phương pháp này có thể được dùng để tạo Linh trưởng chuyển gen.
Chuyển gen vào tiền thể tinh trùng in vitro
Tinh trùng thành thục được tạo ra từ các tế bào gốc thông qua các giai đoạn khác nhau của sự biệt hóa (Hình 2.25). Các tế bào gốc tinh trùng có thể được tách chiết, nuôi cấy in vitro trong một thời gian ngắn và được cấy chuyển vào tinh hoàn nhận. Các tế bào cấy chuyển này hoạt động theo chương trình biệt hóa của chúng làm cho tinh trùng hoạt động chức năng. Tỉ lệ tinh trùng tạo thành từ các tế bào gốc cấy chuyển được tăng lên nhiều nhờ sự xử lý các con đực nhận với bisulfan. Bisulfan là một loại thuốc ngăn cản sự biệt hóa của tế bào gốc tinh hoàn. Protocol này đã được sử dụng một cách thành công để chuyển gen vào tế bào gốc trong quá trình nuôi cấy. Ðiều này đạt được nhờ sử dụng vector retrovirus hiệu quả. Các tế bào gốc cấy chuyển vào con đực nhận đã xử lý bisulfan dẫn đến kết .
 |
Các bước khác nhau của sự biệt hóa tế bào gốc thành tinh trùng
Các tế bào gốc hoặc các tế bào đã biệt hóa một cách cục bộ được tách chiết, nuôi cấy và chuyển DNA chọn lọc vào. Tinh trùng mang DNA ngoại lai này được sử dụng để thụ tinh bằng phương pháp ICSC
Tế bào gốc được tách chiết, nuôi cấy dưới những điều kiện ngăn cản sự biệt hóa của chúng, được chuyển DNA ngoại lai vào, được chọn lọc và đưa vào lại một tinh hoàn nhận, nơi mà chúng biệt hóa. Tinh trùng tạo ra được sử dụng để thụ tinh trứng bằng phương pháp thông thường quả là tạo ra chuột chuyển gen với tỉ lệ cao, khoảng 4%(Nagano, 2001). Phương pháp này là hữu dụng để nghiên cứu ảnh hưởng sinh học của gen trong quá trình thành thục tế bào gốc tinh trùng và để tạo động vật chuyển gen. Có thể suy ra phương pháp này ít thành công hơn đối với các loài lớn hơn chuột. Dường như cần thiết phải sử dụng các tế bào đã được biến nạp cao hơn để tăng cơ hội định cư ở tinh hoàn với một tỉ lệ chấp nhận được.
Chuyển gen vào tiền thể của tinh trùng in vivo
DNA liên kết với thể chuyển nhiễm có thể được tiêm vào các ống sinh tinh (Hình dưới). Một số nhóm nghiên cứu đã thành công trong việc tạo chuột chuyển gen bằng cách sử dụng tinh trùng của các động vật đã được xử lý (Sato, 2002). Những kết quả khích lệ này có hiệu quả vừa phải và hãy còn chưa đạt chuẩn. Hiện chúng đang được cải tiến nhưng chắc chắn là chưa có cách nào làm cho có thể áp dụng rộng rãi phương pháp này đối với các động vật lớn hơn chuột. Quả thực cấu trúc của các ống dẫn tinh khác nhau và việc tiêm DNA là khó. Mặt khác, lượng DNA tiêm vào có thể là rất lớn và khó điều khiển.
 |
| Chuyển gen vào tiền thể của tinh trùng một cách trực tiếp |
DNA bình thường hoặc DNA bám vào thể chuyển nhiễm được tiêm trực tiếp vào các ống sinh tinh. Các tế bào đã hợp nhất DNA ngoại lai sẽ tạo ra động vật chuyển gen sau khi thụ tinh bình thường
Một điểm khác cũng cần được nghiên cứu. Ðó là ở chuột, gen chuyển vào tiền thể của tinh trùng in vivo xảy ra một cách độc lập trong các tế bào khác nhau dẫn đến tạo ra các động vật sơ sinh có sự hợp nhất khác nhau. Ðây là một thuận lợi vì sự hợp nhất khác nhau có thể cho các kiểu hình hơi khác biệt. Với phương pháp này, các nhà nghiên cứu có thể đánh giá các dòng động vật chuyển gen phức tạp từ một thí nghiệm đơn giản.
Kỹ thuật viên gen (Gene pill)
Kỹ thuật viêm gen một phương pháp điều trị bệnh bằng liệu pháp gen thông qua đường uống thuốc.
Một lượng DNA liệu pháp (dạng plasmid hay phức hợp DNA-peptid) được bọc bởi một màng lipid hỗn hợp đặc hiệu như màng bọc các viên thuốc thông thường tạo ra viên gen. Viên gen được đưa vào cơ thể theo đường miệng bằng cách uống. Sau khi được được phóng thích, gen liệu pháp được hấp thụ qua màng đi vào tế bào biểu mô ruột. Ở đây gen liệu pháp được phiên mã và dịch mã thành protein dược phẩm. Protein dược phẩm tiết vào máu, đến các mô bệnh để ức chế sự hoạt động của các gen bệnh .
Kỹ thuật viên gen là một phương pháp mới (được cấp bằng phát minh vào ngày 3/5/2001) lần đầu tiên được sử dụng để chữa bệnh tiểu đường bằng cách sử dụng một viên gen được tạo thành từ DNA mã hóa inssulin. Phương pháp này đã khắc phục được các hạn chế của các phương pháp truyền thống như vấn đề liều lượng và phân phối thuốc. Nó có thể cách mạng hóa liệu pháp gen và cho các bệnh nhân một sự chọn lựa để đưa insulin vào cơ thể hàng ngày.
Tuy nhiên, tính có ích của viên gen sẽ phụ thuộc vào sự biểu hiện và phân phối của gen trong các tế bào ruột non và hãy còn chưa chắc chắn là có thích hợp đối với các protein cần thiết với liều lượng khớp một cách tinh vi không.
 |
| Sơ đồ cơ chế hoạt động của viên gen |
- 1Viên gen phân phối DNA đến ruột non
- DNA được hấp thụ vào các tế bào ruột
- Protein dược phẩm tổng hợp trong các tế bào
- Protein dược phẩm tiết vào máu
Kỹ thuật viên gen khai thác một cách tích cực khoảng thời gian sống ngắn của các tế bào biểu mô và tính có lợi của sự phân chia một cách nhanh chóng của các tế bào đích xếp thành hàng trong ruột non. Về mặt lý thuyết, liệu pháp gen thông qua đường uống có thể phân phối gen tổng hợp bất cứ protein nào cho một loại tế bào đơn trong ruột non, đáp ứng được yêu cầu tìm ra vector hoặc chiến lược biến nạp mới cho mỗi một loại tế bào đích. Tuy nhiên phương pháp này cho hiệu quả chưa cao do sự sử dụng các tế bào ruột non làm các tế bào đích bị giảm bởi nhiều nhóm tế bào có thời gian sống ngắn (2-3 ngày), môi trường acid và DNAse trong hệ dạ dày ruột. Mặt khác, viên gen chỉ có thể mang các gen ngoại lai có kích thước nhỏ. Hiện nay người ta mới chỉ tạo ra được một số loại viên gen sử dụng trong điều trị thử nghiệm. Trong tương lai viên gen sẽ trở thành một kỹ thuật có hiệu quả để điều trị bệnh bằng liệu pháp gen.
Nguồn tham khảo:
https://voer.edu.vn/m/cac-phuong-phap-chuyen-gen/993889db







Không có nhận xét nào:
Đăng nhận xét